Первое описание альбуминового диализа в системе одного перехода альбуминового диализата (SPAD) в сочетании с адсорбцией цитокинов при фульминантной форме печеночной недостаточности и гемофагоцитарном синдроме на фоне генерализованной инфекции Herpes Simplex Virus 1
Фриммель С. (Frimmel S), Шиппер Дж. (Schipper J), Хеншель Дж. (Henschel J), Тсуи Т.Я. (Tsui TY), Митцнер С.Р. (Mitzner S.R.), Кобалль С. (Koball S)
Отделение нефрологии, Медицинский факультет медицинского центра Университета г. Росток (Rostock University Medical Center), Росток, Германия Журнал Liver Transpl. 2014, сентябрь 19
К ИЗДАТЕЛЯМ:
Острая печеночная недостаточность (ОпечН) -‐ достаточно редкое, угрожающее жизни осложнение инфицирования herpes simplex virus (HSV), которое может возникнуть у иммунокомпетентных пациентов. Трансплантация печени является ultima ratio (последним доводом) в случаях прогрессирования ОПечН, несмотря на антивирусную терапию. 1 Для поддержания пациента до трансплантации терапевтической опцией является экстракорпоральная поддержка печени с помощью молекулярной адсорбирующей рециркулирующей системы MARS (Mars, Gambro, Лунд, Швеция)2. В подобных случаях существует мало данных о применении альбуминового диализа в системе одного перехода альбуминового диализата (SPAD)3. Гемофагоцитарный лимфогистиоцитоз – тяжелый гипервоспалительный синдром, который может возникнуть при многих условиях. 4
Исследования на животных, отчеты о клинических случаях и предварительный данные из клинических испытаний на септических пациентах продемонстрировали, что снижение уровня цитокинов в крови, достигнутое с помощью экстракорпоральной адсорбционной системы CytoSorb, которая содержит крове-‐совместимые пористые горошины полимера (CytoSorb, Монмаут Джанкшн, штат Нью-‐Джерси), может эффективно уменьшать воспалительный ответ при сепсисе и, возможно, улучшать клинический исход. 5,6
ОТЧЕТ О КЛИНИЧЕСКОМ СЛУЧАЕ
Женщина, 50 лет, была доставлена в стационар с острым гепатитом и ОпечН. Трансвенозная биопсия печени показала острый некроз клеток печени. HSV1 был определен в качестве возбудителя, была начата антивирусная терапия ацикловиром. Так как печеночная недостаточность прогрессировала, пациентку перевели в отделение интенсивной терапии. Развился синдром полиорганной недостаточности, печеночная кома, тяжелая коагулопатия, острая почечная недостаточность с развитием анурии, респираторная недостаточность и артериальная гипотензия. Пациентка была включена в программу Eurotransplant для срочной пересадки печени. Гиперферритинемия до 266,000 μг/л (диапазон нормальных значений = 13-300 μг/л) в сочетании с панцитопенией и высоким уровнем растворимого рецептора интерлейкина-2 (IL-‐2) в плазме крови (6815 ЕД/мл, диапазон нормальных значений = 223‐710 ЕД/мл) вызывали подозрения на вторичный вирус-ассоциированный гемофагоцитарный лимфогистиоцитоз. Была проведена биопсия костного мозга. Гистологическое исследование выявило высокое число активированных макрофагов, сопровождащихся гранулоцитозом и эритроцитозом, что указывало в пользу диагноз вторичного вирус-ассоциированного гемофагоцитарного лимфогистиоцитоза на фоне HSV1.
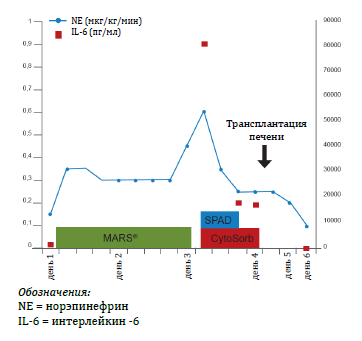
Были начаты гемодиализ и экстракорпоральная поддерживающая терапия печени с помощью молекулярной адсорбирующей рециркулирующей системы MARS в течение 6 часов в первый день и 19 часов на вторые сутки. Усугубляющийся циркуляторный коллапс с повышением потребности в норэпинефрине (максимум = 0.6 μг/кг/мин) и чрезмерно возросшие уровни концентрации маркеров воспаления (IL-6 и ферритин) указывали на развитие синдрома системного воспалительного ответа. В этой связи экстракорпоральная терапия была заменена на постоянный вено-венозный гемодиализ, со стандартным аппаратом для гемодиализа был проведен альбуминовый диализ в системе одного перехода альбуминового диализата (SPAD). Использовался аппарат Multifiltrate, Fresenius Medical Care, Bad Homburg, Германия) c высокоплотной полисульфоновой мембраной (Ultraflux AV100S, Fresenius medical Care). Стандартный диализный раствор был обогащен 20% раствором человеческого альбумина до достижении итоговой концентрации альбумина 2% (поток диализата = 1500 мл/час; 12 часов терапии). После 12 часов терапии SPAD был продолжен стандартный вено-венозный гемодиализ. Система гемоадсорбции CytoSorb была установлена до фильтра для диализа (общая продолжительность сессии = 20 часов) для повышения адсорбции цитокинов. Проводилась регионарная цитратная антикоагуляция. До сессии терапии с помощью CytoSorb концентрация IL-6 составляла 81.059 пг/мл (нормальные значения < 7.00 пг/мл). Спустя 12 часов терапии CytoSorb она упала до 17.177 пг/мл. Дозировка норэпинефрина была снижена до 0.25 μг/кг/мин. Клинического ухудшения состояния пациентки не произошло. Что интересно, во время комбинации SPAD и CytoSorb было достигнуто снижение концентрации билирубина, в то время как при терапии только с помощью MARS показатель билирубина повышался. Успешная ортотопическая трансплантация печени была проведена на 4‐ый день пребывания в отделении интенсивной терапии. Через 2‐е суток после трансплантации под иммуносупрессией с помощью препаратов такролимус (Tacrolimus) и преднизон (Prednisone) уровни ферритина и IL-‐6 в плазме снизились далее до 7202 μг/л и 47.2 пг/мл, соответственно (Рис.1).
ДИСКУССИЯ
Насколько нам известно, это первый отчет о гемоадсорбции с помощью CytoSorb, применявшейся в сочетании со SPAD у пациента, находящегося в листе ожидания на трансплантацию печени, с острым повреждением печени и вероятным гемофагоцитарным лимфогистиоцитозом, а также острым синдромом системного воспалительного ответа. Значительное снижение уровня IL‐6 и билирубина и снижение потребности в вазопрессорах были основными результатами терапии. Адсорбция провоспалительных цитокинов, снижающая их концентрацию для коррекции системного воспалительного ответа и детоксикации, может оказаться полезным инструментом терапии острой печеночной недостаточности и тяжелых гипервоспалительных синдромов, таких как гемофагоцитарный лимфогистиоцитоз. Терапия была безопасной и хорошо переносилась пациентом, неблагоприятных событий не зарегистрировано. Многоцентровые исследования требуются для подтверждения польрисзы терапии.
<
Сильвиус Фриммель (Silvius Frimmel), дипломированный врач 1 Ян Шиппер (Jan Schipper), дипломированный врач 1
Йорг Хеншель (Joerg Henschel), дипломированный врач 2
Тсунг Ю Тсуи (Tsung Yu Tsui), дипломированный врач, кандидат наук 3
Штеффен Р. Митцнер (Steffen R. Mitzner), дипломированный врач, кандидат наук 1,4 Себастиан Кобалль (Sebastian Koball), дипломированный врач 1
1 Отделение нефрологии, медицинский факультет
2 Отделение интенсивной терапии, Медицинский Факультет
3 Секция онкологической хирургии и трансплантации Медицинский центр университета г. Росток, Росток, Германия
4 Палата экстракорпоральной иммуномодуляции, Институт терапии клеток и иммунологии Frauhofer, Росток, Германия
РЕФЕРЕНСЫ
1. Norvell JP, Blei AT, Jovanovic BD, Levitsky J. Herpes simplex virus hepatitis: an analysis of the published literature and institutional cases. Liver Transpl 2007;13: 1428-1434.
2. Saliba F, Camus C, Durand F, Mathurin P, Letierce A, Delafosse B, et al. Albumin dialysis with a noncell artificial liver support device in patients with acute liver failure: a randomized, controlled trial. Ann Intern Med 2013;159:522-531.
3. Karvellas CJ, Bagshaw SM, McDermid RC, Stollery DE, Bain VG, Gibney RT. A case-control study of single-pass albumin dialysis for acetaminophen-induced acute liver failure. Blood Purif 2009;28:151-158.
4. Janka GE, Lehmberg K. Hemophagocytic syndromes—an update. Blood Rev 2014;28:135-142.
5. Peng ZY, Carter MJ, Kellum JA. Effects of hemoadsorption on cytokine removal and short-term survival in septic rats. Crit Care Med 2008;36:1573-1577.
6. Mitzner SR, Gloger M, Henschel J, Koball S. Improvement of hemodynamic and inflammatory parameters by combined hemoadsorption and hemodiafiltration in septic shock: a case report. Blood Purif 2013;35:314-315.

