Экстракорпоральная гемоперфузия в качестве потенциальной терапии критического накопления ривароксабана в организме
Koertge A, Wasserkort R, Wild T, Mitzner S. Extracorporeal Hemoperfusion as a Potential Therapeutic Option for Critical Accumulation of Rivaroxaban.
Blood Purif. 2018;45(1-3):126-128. doi: 10.1159/000484923. Epub 2017 Dec 21. PMID: 29402788.
Ссылка на оригинал: https://pubmed.ncbi.nlm.nih.gov/29402788/
Благодаря эффективности, легкости дозирования и безопасности, пероральный антикоагулянт ривароксабан применяется в практике все чаще, например, для предотвращения инсультов, системной эмболии у пациентов с неклапанной фибрилляцией предсердий [1], а также в терапии тромбозов глубоких вен и эмболии легочной артерии. Средняя пиковая терапевтическая концентрация ривароксабана в плазме крови варьируется от 46 до 270 мкг/л, в зависимости от назначения [3]. Однако, есть опасения по поводу накопления этого препарата в организме пациентов в случаях передозировки, а также если у пациента имеются нарушения ренального клиренса. В таких обстоятельствах риск возникновения кровотечений повышается [4]. Ривароксабан хорошо связывается с белками плазмы (92-95% [3]), и причисляется к недиализируемым веществам. Такая характеристика подтверждается исследованием Dias et al. [5]. В связи с тем, что связывание с белками не является ограничивающим фактором для проведения гемоперфузии, до настоящего момента считалось возможным удаление ривароксабана с помощью распространенных углеродных картриджей, однако, экспериментальных данных, подтверждающих это положение, до сих пор не опубликовано [7]. Тогда как препарат Andexanet alfa может потенциально служить ингибитором ривароксабана путем опосредованного ингибирования фактора Xa, он до настоящего времени не одобрен к применению [8]. В случае обширных кровотечений, связанных с приемом ривароксабана, или при неотложных вмешательствах с высоким риском развития кровотечений, необходимо иметь в запасе эффективные контрмеры.
Мы представляем результаты экспериментальной работы по удалению ривароксабана из цельной крови в контуре гемоперфузии с адсорбером CytoSorb (Cytosorbents Europe, Германия). В настоящее время CytoSorb используется для работы с пациентами с тяжелыми инфекциями и сепсисом (цитокиновым штормом). Для удаления высокой концентрации ривароксабана (571± 20 мкг/л) из плазмы цельной крови, антикоагулированной цитратом (1000 мл, скорость кровотока 40 мл/мин), мы использовали модель адсорбера, содержащую 60 мл адсорбента в системе рециркуляции in vitro. Гемоперфузия проводилась на протяжении 120 минут (рис. 1а). Принцип работы: молекулы улавливаются внутренними порами адсорбента при помощи неспецифичного гидрофобного взаимодействия, тогда как растворенные вещества с молекулярным весом, равным или превышающим альбумин, в частности факторы свертывания, исключаются из спектра адсорбируемых веществ [9]. Мониторинг pH во время экспериментов проводился с помощью анализатора газов крови ABL90 FLEX (Radiometer, Дания). pH поддерживался на уровне от 7.35 до 7.45 при помощи Трис-буфера. Нагрев крови обеспечивался инфракрасным нагревателем элементов крови (Fluido; The Surgical Company; Германия). Концентрации ривароксабана определялись фотометрическим методом с использованием образцов хромогенного субстрата антифактора Xa (BIOPHEN Heparin LRT; HYPHEN BioMed, Франция). Использовались калибраторы концентраций ривароксабана на 0,276 и 497 нг/мл. Анализы проводились в центральной лаборатории Медицинского Университета г. Росток.
Через час после рециркуляции 91.6% ривароксабана было удалено из крови, что привело к снижению его концентрации в плазме до 47.6 мкг/л (рис.1b). Та же самая система рециркуляции без CytoSorb показала только незначительное снижение концентрации ривароксабана после 5 часов циркуляции. Финальная концентрация ривароксабана при применении CytoSorb превышала 30 мкг/л, при которых в экстренных случаях рекомендован пероральный прием антидота [8]. Через 120 минут после завершения гемоперфузии произошло насыщение 60 мл модели CytoSorb, что подтверждалось совсем небольшой разницей концентраций на входе и выходе, снижением клиренса ривароксабана из плазмы и экстракционного индекса (рис. 1с). Таким образом, применение еще одной уменьшенной модели CytoSorb могло быть эффективным для более быстрого удаления таких высоких концентраций препарата, как мы использовали в настоящем исследовании. Однако, для нормальных терапевтических концентраций ниже 300 мкг/л мы ожидаем снижения концентрации ривароксабана в плазме крови ниже критического порога с помощью всего 1 адсорбера за 30-60 минут. Принимая во внимание низкий объем распределения препарата (0.62 л/кг) и конечный период полувыведения (5-13 часов) [3], настоящие результаты позволяют предположить, что гемоадсорбция с помощью CytoSorb может представлять собой подходящее средство для быстрого реверса антикоагуляционного эффекта ривароксабана in vivo. Дополнительное тестирование in vivo требуется для верификации полученных результатов 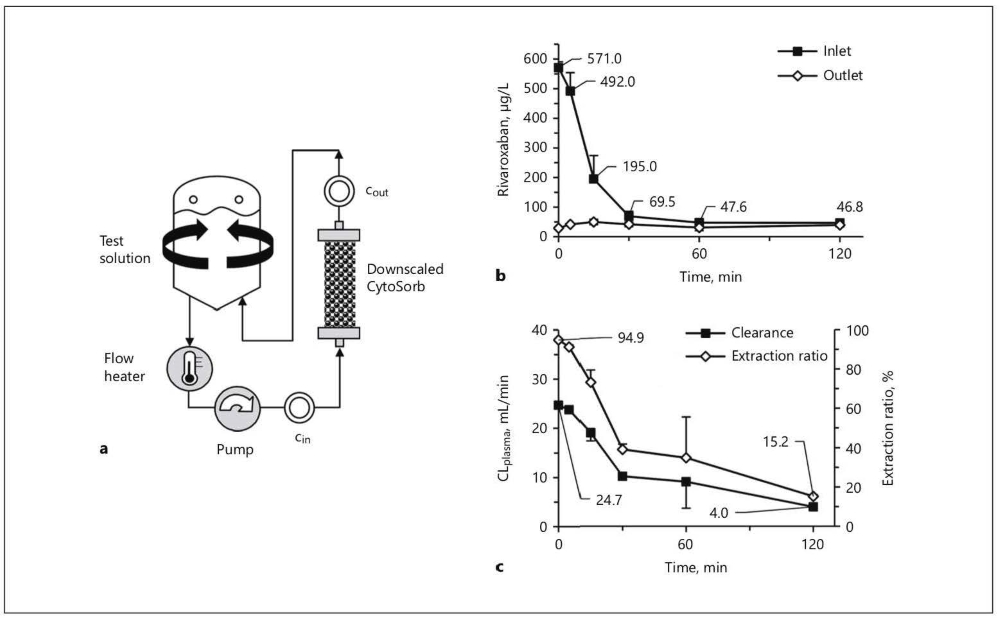
Рис. 1 a Схема модели рециркуляции in vitro. b Концентрации ривароксабана в плазме на входе и выходе, (с) коэффициент очищения Re = (cin – cout)/cin и клиренс из плазмы CL = QB х (1-Hct) х Re [7] за 120 мин, во время которых происходила рециркуляция крови сквозь миниатюрную модель CytoSorb (среднее ± стнд отклонение, n=2). Значения CL были получены, принимая во внимание среднюю концентрацию гематокрита, рассчитанную с помощью значений, измеренных в начале и конце каждого эксперимента (0.349 ±0.018, n=4).
Благодарности
Авторы хотят отметить экспериментаторский труд Benjamin Heskamp и Manuel Folk, а также поблагодарить доктора Christine Burstein и доктора Jolanta Majcher-Peszynska за полезные комментарии в отношении дизайна экспериментов и проведение анализа ривароксабана.
Раскрытие информации
Этому исследованию была оказана финансовая поддержка Cytosorbents Europe. Миниатюризированные адсорберы были предоставлены Cytosorbents Europe. Кроме вышеуказанного, авторы декларируют отсутствие конфликта интересов.
Ссылки
1 Fox KA, Piccini JP, Wojdyla D, Becker RC, HAlperin JL, Nessel CC, Paolini JF, Hankey GJ, Mahaffey KW, Patel MR, Singer DE, Califf RM: Prevention of stroke embolism with rivaroxaban compared with warfarin in patients with non-valvular atrial fibrillation and moderate renal impairment. Eur. Heart 2011;32:2387-2394.
2 Goldhaber SZ, Bounameaux H: Pulmonary embolism and deep vein thrombosis. Lancet 2012;379:1835-1846.
3 Mueck W, Stamfuss J, Kubitza D, Becka M:Clinical pharmacokinetic and pharmacodynamics profile of rivaroxaban. Clin Pharmacokinet 2014;53:1-16.
4 Chan KE, Giugliano RP, Patel MR, Abramson S, Jardine M, Zhao S, Perkovic V, Maddux FW, Piccini JP: Nonvitamin K anticoagulant agents in patients with advanced chronic kidney desease or on dialysis with AF. J Am Coll Cardiol 2016;67:2888-2899

