Использование новой системы гемоадсорбции для удаления цитокинов в качестве вспомогательной терапии для пациентов с септическим шоком и полиорганной дисфункцией: описание клинического случая
Решма Басу (Reshma Basu), Сунджай Патак1 (Sunjay Pathak), Джоти Гоял1 (Jyoti Goyal), Раджив Чондри1 (Rajeev Chaundry), Рати Б. Гоэль1 (Rati B. Goel), Анил Барваль1 (Anil Barwal)
Индийский журнал медицины критических состояний (Indian Critical Care Medicine) Декабрь 2014 Выпуск 18 Издание 12
CytoSorb® (производитель CytoSorbents Corporation, США) – новая система гемоадсорбции для удаления цитокинов. Цель настоящего исследования оценить клиническое применение CytoSorb для ведения пациентов с септическим шоком. Мы использовали эту систему в качестве вспомогательной терапевтической меры для стабилизации молодой пациентки с полиорганной недостаточностью и тяжелым сепсисом и септическим шоком. 36-летняя пациентка была госпитализирована с жалобами на недомогание, боль во всем теле и затрудненное дыхание. История болезни включала сахарный диабет 2-го типа, обструктивное апноэ сна, гипертензию, гипотериоз и морбидное ожирение. Был поставлен диагноз септический шок, полиорганная недостаточность и низкая перфузия. Система гемоадсорбции CytoSorb® применялась в качестве средства очистки крови. Оценки по шкале хронической органной недостаточности APACHE, шкале нарушения функции нескольких органов MODS и шкале оценки последовательного отказа органов SOFA были проведены до и после применения системы CytoSorb. Система CytoSorb может рассматриваться в качестве вспомогательной терапии для пациентов с септическим шоком.
Ключевые слова:
CytoSorb, гемоадсорбция, септический шок, синдром системного воспалительного ответа.
Введение
Уровень смертности пациентов с септическим шоком все еще находится на уровне 60%. Более часто смерть наступает в отделениях интенсивной терапии.[1] Для улучшения клинического исхода пациентов с сепсисом исследуются экстракорпоральные методики очистки крови. Гемоадсорбция с помощью CytoSorb® (производства CytoSorbents Corporation, США) является современной технологией, которая показала быструю элиминацию in vivo и in vitro многих ключевых цитокинов, включая интерлейкин-‐6 (IL-6), интерлейкин-‐1 (IL-‐1), фактор некроза опухолей (TNF) и интерлейкин-‐10 (IL-‐10), которые невозможно отфильтровать, применяя существующие технологии очистки крови.[2-‐5] Системы CytoSorb® состоят из пористых горошин полимерного адсорбента размером чуть больше крупинки соли, высокосовместимых с кровью. Горошины также обладают свойством селекции размера, они адсорбируют молекулы размером от 10000 до 50000 Да. Во время очистки крови токсичные молекулы малого размера попадают в поры и каналы на поверхности каждой горошины и задерживаются на внутренней поверхности горошин в результате гидрофобных взаимодействий с нейтральной липофильной поверхностью полимера, в то время как более крупные эссенциальные белки крови проходят фильтр и возвращаются назад пациенту.[6] Митцнер (Mitzner) et al сообщал об эффективности и хорошей переносимости терапии CytoSorb пациентом с хронической почечной недостаточностью и септическим шоком.[7] Мы сообщаем о применении CytoSorb® для стабилизации пациентки с септическим шоком, низким перфузионным статусом и полиорганной недостаточностью.
Отчет о клиническом случае
36-‐летняя женщина поступила в наше лечебное учреждение с жалобами на боль во всем теле в течение 3-‐х последних дней, а также недомогание и затруднение дыхания в течение 2-‐х дней перед обращением в медицинское учреждение. История болезни пациентки содержит сахарный диабет 2-‐го типа, обструктивное апноэ сна, гипертензию, гипотериоз и морбидное ожирение. При осмотре зарегистрирована тахикардия (120 уд./мин.), учащенное дыхание (36 дых./мин.) и лейкоцитоз (количество лейкоцитов > 52 000). Мы подозревали инфекцию мочевых путей (количество гнойных клеток – 12-‐15). Была начата терапия антибиотиками (меропенем (meropenem) 500 мг 3 раза в день), прописаны вазопрессоры [Таблица 1], проводилось восстановление объема жидкости, потребовалась искусственная вентиляция. Состояние пациентки продолжало ухудшаться, диурез снижался. Ее интубировали в течение 4 часов после поступления, через 6 часов наступила анурия. Через 24 часа после поступления пациентки оценка ее состояния по международной шкале SOFA составляла 15 баллов, по шкале MODS -‐10, по шкале APACHE II – 30.
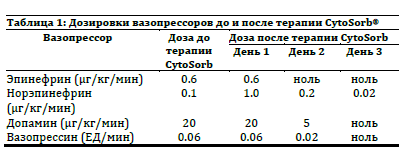
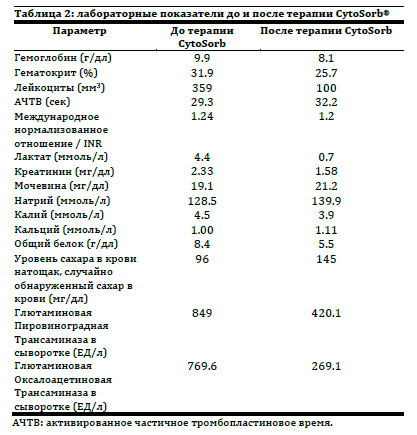
Был поставлен диагноз септический шок (уросепсис) с низким перфузионным статусом и полиорганная недостаточность (острый респираторный дистресс-‐синдром (ОРДС), острое повреждение почек, артериальная гипотензия). Через 16 часов после поступления начата постоянная почечно-‐заместительная терапия в комбинации с CytoSorb. Терапия проводилась 24 часа. Скорость кровотока поддерживалась на уровне 250 мл/мин. Антикоагуляция проводилась с помощью гепарина для поддержания АЧТВ (активированное частичное тромбопластиновое время) на уровне 30-‐40 секунд. Через 12 часов в состоянии пациента наступили гемодинамические улучшения. Одновременно с инотропной поддержкой и CytoSorb® проводились внутривенные инъекции гидрокортизона и использовались другие виды терапии. После этого периода стало возможным отменить норадреналин, постепенно снимали и остальную вазопрессорную поддержку [Таблица 1]. Кортикостероды (гидрокортизон внутривенно) в дозировке 100 мг три раза в сутки использовались до тех пор, пока пациентку не перевели на инотропную поддержку. Состояние пациентки стабилизировалось в течение 3 суток, в это время система CytoSorb® применялась ежедневно. За этот период увеличился диурез, произошла положительная динамика в параметрах вентиляции. Оценка по шкале SOFA составила 4 балла, по шкале MODS – 5 баллов, а по шкале APACHE II – 7. Лабораторные показатели до и после терапии с помощью системы CytoSorb находились в границах диапазона нормальных значений, подробно эти показатели представлены в Таблице 2.
Обсуждение
Мы сообщаем об одном из первых случаев комбинации стандартной терапии с терапией CytoSorb® в качестве вспомогательной при ведении пациента с септическим шоком и полиорганной недостаточностью. Терапия хорошо переносилась пациентом, после 3-‐х суток пациента удалось стабилизировать.
Пациенты с септическим шоком требуют агрессивной терапии в сочетании с искусственной вентиляцией легких, вазопрессорной поддержкой и почечно-‐заместительной терапией.[1] На основании клинико-‐экспериментальных данных гемоадсорбция может быть полезной для данной категории пациентов. Однако в настоящее время доказательная база небольшая. На животных моделях с септическим шоком гемоадсорбция с помощью системы CytoSorb® ассоциировалась со снижением воспаления и значительным улучшением выживаемости. [8] Исследование in-vitro, проведенное Пенгом (Peng) et al показало, что гемоадсорбция с применением системы CytoSorb® снижает уровень концентрации противовоспалительных цитокинов (TNF, IL-‐1β, IL-‐6 и IL-‐10) и значительно улучшает среднее артериальное давление (p < 0.05) и общий показатель выживаемости (p < 0.01) у крыс с сепсисом, индуцированным перевязкой слепой кишки и проколом.[5] Риммеле (Риммеле) et al провели гемоадсорбцию ex-‐vivo на образцах крови, взятых у 21 пациента с септическим шоком и 12 здоровых волонтеров. Они наблюдали повышенную регуляцию интерлейкина 8 (IL-‐8) и модуляцию клеточно-‐опосредованного иммунитета при гемоадсорбции, а это могло бы помочь уменьшить повреждения органов.[9,10]
Технология CytoSorb® подразумевает использование горошин адсорбента, состоящих из биосовместимого кополимерного дивинилбензола. Это горошины захватывают и поглощают цитокины и другие молекулы среднего молекулярного веса. Первое рандомизированное контролируемое исследование, выполненное с применением системы CytoSorb® у септических пациентов с острым повреждением легких отметило значительное снижение концентрации цитокинов и хорошо переносилось пациентами. [3] У нашего пациента мы не заметили никаких неблагоприятных эффектов, гемограмма и клиническая биохимия до и после применения CytoSorb оставались в пределах нормальных значений [Таблица 2].
CytoSorb® эффективен для снижения постоперационного синдрома системного воспалительного ответа.[11] В отчете о клиническом случае, представленном Хетц (Hetz) et al, у женщины 60 лет с переломом руки после операции развилась инфекция хирургической раны, прогрессировавшая в некротический фасциит, сопровождающийся септическим шоком. После 4 суток терапии CytoSorb® было отмечено значительное снижение уровня концентрации интерлейкина 6 (IL-‐6) и общее улучшение состояния пациента. [12] Похожим образом, различные другие обзоры клинических случаев использования CytoSorb® на человеке также дают информацию о том, что терапия CytoSorb® помогла снизить несколько медиаторов воспаления у пациентов с гиподинамическим и пневмогенным септическим шоком. [13,7]
В настоящем исследовании сообщается об удачном исходе применения CytoSorb® в качестве вспомогательной терапии в случае септического шока и полиорганной недостаточности. Пациентка имела высокий риск смертности (оценка по шкале APACHE II – 30 баллов). Пациентке проводили стандартную терапию наряду с применением вспомогательной терапии, в течение которой провели три последовательных сеанса c помощью гемоадсорбционной системы CytoSorb®. CytoSorb® мождет выступать в качестве опции для неотложной терапии пациентов с полиорганной недостаточностью. Тем не менее, необходимы дальнейшие проспективные рандомизированные исследования для утверждения преимуществ этой терапии в качестве вспомогательной при септическом шоке.
Ссылки
1. Аннане Д. (Annane D), Аегертер П. (Aegerter P), Ярс-Гинцестре М.К. (Jars-‐Guincestre MC), Гидет Б. (Guidet B), The (CUB-‐Réa). Современная эпидемиология септического шока: Реестр пользователей базы данных поступлений в реанимацию. Журнал “Американский журнал респираторной и интенсивной медицины” (American Journal of Respiratory and Critical Care ). 2003;168:165-‐72.
2. Танигучи Т. (Taniguchi T), Хирай Ф. (Hirai F), Такемото Й (Takemoto Y), Тсуда К. (Tsuda K), Ямамото К (Yamamoto K), Инаба Х. (Inaba H), et al. Новый адсорбент циркулирующих токсинов и цитокинов: Эффект прямой гемоперфузии с колонкой СTR (пр-‐ва Kaneka) при терапии экспериментальной эндотоксемии. Журнал “Медицина критических состояний” (Critical Care Medicine) 2006;34:800-‐6.
3. Шэдлер Д. (Schädler D), Порцелиус К. (Porzelius C), Йоррес А. (Jörres A), Маркс Г. (Marx G), Майер-‐Хелльманн (Meier-‐Hellmann A), Путенсен К (Putensen C), et al. Мультицентровое рандомизированное контролируемое исследование экстракорпоральной системы цитокиновой гемоадсорбции у пациентов с септическим шоком. Журнал “Критические состояния“ (Critical Care) 2013; 17:62.
4. Танигучи Т. (Taniguchi T), Курита А. (Kurita A), Мукава Ц (Mukawa C), Ямамото К. (Yamamoto K), Инаба Х. (Inaba H). Дозозависимые эффекты прямой гепоперфузии с применением колонки для адсорбции цитокинов для терапии экспериментальной эндотоксемии. Журнал “Интенсивная терапия” (Intensive Care Medicine) 2007;33:529-‐33.
5. Пенг Ж.Ю. (Peng ZY), Картер М. Ж.(Carter MJ), Келлум Ж.А. (Kellum JA). Эффективность гемоадсорбции для удаления цитокинов и ее влияние на краткосрочную выживаемость у крыс с сепсисом. Журнал “Медицина критических состояний” (Critical Care Medicine) 2008;36:1573-‐7
6. Оноре П-‐М. (Honore PM), Якобс Р. (Jaсobs R), Йоаннес-‐Боя О. (Joannes-‐Boyau O), Де Регт Дж (De Regt J), Де Ваеле Е.(De Waele E), ван Корп В. (van Gorp V), et al. Недавно разработанные мембраны для постоянной почечно-заместительной терапии при сепсисе и синдроме системного воспалительного ответа – прагматичный подход для интенсивистов-‐практиков, охватывающий самые последние нововведения: системно-‐структурированный обзор. Журнал «ASAIO Journal» 2013;59:99-‐106.
7. Митцнер Ш.-‐Р. (Mitzner SR), Глогер М. (Gloger M), Хеншель Й. (Henschel J), Кобалль С. (Koball S). Улучшение гемодинамических параметров и показателей воспаления путем комбинации гемоадсорбции и гемофильтрации при септическом шоке: отчет о клиническом случае. Журнал «Blood Purification» 2013;35:314-‐5.
8. Келлум Дж.-‐А. (Kellum JA), Сонг М. (Song M), Венкатараман Р. (Venkataraman R). Гемоадсорбция удаляет фактор некроза опухолей, интерлейкин-‐6 и интерлейкин-‐10, снижает связывание ДНК с помощью ядерного фактора каппа-‐би и улучшает краткосрочную выживаемость при летальной эндотоксемии. Журнал “Медицина критических состояний” (Critical Care Medicine) 2004;32:801-‐5.
9. Риммеле Т. (Rimmelé T), Кайнар А.-‐М. (Kaynar AM), Мак Лолин Ж.-‐Н. (McLaughlin JN), Бишоп (Ж.-‐В.) Bishop JV, Федорчак М.-‐В.) Fedorchak MV, Часуван А. (Chuasuwan A), et al. Захват лейкоцитов и модуляция клеточно-‐опосредованного иммунитета во время сепсиса у человека: исследование ex-vivo. Журнал “Критические состояния“ (Critical Care) 2013;17:R59.
10. Кумагаи Т. (Kumagai T), Такеяма Н. (Takeyama N), Ябуки Т. (Yabuki T), Харада М. (Harada M), Мики Ю. (Miki Y), Каноу Х. (Kanou H), et al. Аферез активированных лейкоцитов с помощью фильтра иммобилизованного полимиксина B у пациентов с септическим шоком. Журнал «Шок» (Shock) 2010;34:461-‐6.
11. Борн Ф. (Born F), Пихльмайер М. (Pichlmaier M), Петерсс С. (Peterss S), Кхаладж Н. (Khaladj N), Хагль С (Hagl C). Синдром системного воспалительного ответа в кардиохирургии: Новая терапия с применением цитокиновых адсорберов. Немецкий журнал «АКШ» (EKZ) 2014;23:41-‐6.
12. Хетц Х. (Hetz H), Бергер Р. (Berger R), Рекнагель П. (Recknagel P), Штельцер Х. (Steltzer H). Новая терапия септического шока на фоне некротического фасициита, вызванного β-‐ гемолитическим стрептококком, с помощью адсорбции цитокинов. Журнал «Международный журнал искусственных органов» (International Journal of Artificial Organs) 2014;37:422-‐6.
13. Брахт Х. (Bracht H), Шнайдер М. (Schneider M), Вайсс М. (Weiss M), Георгиев М. (Georgieff M), Барт Е. (Barth E). Модель извлечения цитокинов с помощью адсорбционной системы CytoSorb® при септическом шоке, вызванном candida albicans. Журнал «Инфекция» (Infection) 2013;41:1-‐90.

